酸素
集め方 どの集め方(上方置換・下方置換・水上置換)
水上置換 酸素は水にとけにくい
作り方 必要な液体と固体
うすい過酸化水素水と二酸化マンガン
性質1 酸素は空気よりも( 重い・軽い )
重い 空気の1.1倍
性質2 酸素は( 燃える・燃えない )
燃えない 酸素はものを燃やす性質(助燃性)があるが、酸素自体は燃えない。
二酸化炭素
作り方 必要な液体と固体
塩酸と石灰石(炭酸カルシウム) 二酸化炭素は石灰石にふくまれている
性質1 二酸化炭素は空気よりも( 重い・軽い )
重い 空気の1.5倍
性質2 二酸化炭素は水に( とけやすい・少しとける・とけにくい )
少しとける 冷水1Ⅼに、二酸化炭素1Ⅼ以上とける。ただ、アンモニアが非常にとけるので、二酸化炭素は「少し」になる。
性質3 二酸化炭素を調べる水溶液は?(二酸化炭素と反応して白くにごる)
石灰水(水酸化カルシウム水溶液)
性質4 石灰水と反応してできた白い固体の名前は?
炭酸カルシウム
集め方1 二酸化炭素をたくさんあつめるには(上方置換・下方置換・水上置換)
下方置換 二酸化炭素は水に少しとけるので、下方置換が原則。
集め方2 二酸化炭素の発生量を調べるときは、図の装置。なぜ、空のフラスコが真ん中にあるのか?
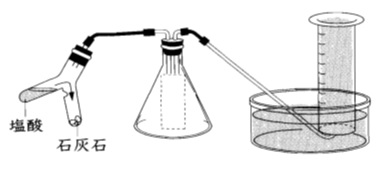

水にとけにくい空気と置き換えて発生量を図るため。 二酸化炭素を直接水中に発生させると、かなりとけてしまうので正確な発生量がはかれない、そこで、発生した二酸化炭素を中央のフラスコに送り、同じ量の空気を水に押し出して発生量を調べる。
水素
作り方1 塩酸にとけて水素を発生させる金属は? (アルミ・鉄・亜鉛・銅)
アルミ・鉄・亜鉛
作り方2 常温の水酸化ナトリウム水溶液にとけて水素を発生させる金属は? (アルミ・鉄・亜鉛・銅)
アルミ
作り方3 塩酸とアルミで水素を作るとき、水素はどちらから発生? ( 塩酸・アルミ )
塩酸 塩酸にとけているのは塩化水素
性質1 水素は空気よりも( 重い・軽い )
軽い 水素は最も軽い金属
性質2 水素は水に( とけやすい・少しとける・とけにくい )
とけにくい 酸素よりもっと溶けにくい
性質3 水素は燃えると何になる?
水
集め方 水素の集め方は? ( 上方置換・下方置換・水上置換 )
水上置換 水素は水にとけにくいので、水上置換
アンモニア
性質1 アンモニアは空気よりも( 重い・軽い )
軽い
性質2 アンモニアは水に( 非常によくとける・少しとける・とけにくい )
非常によく溶ける 冷水1lに1000l以上とける。気体で最も溶けやすい。
性質3 アンモニアは、どちらの水にとけやすい?( 冷たい水・あたたかい水 )
冷たい水 気体はすべて、冷たい水の方が溶けやすい
性質4 アンモニアは、ある液を近づけると、白い煙が出ます。この液の名前は?
塩酸 アンモニアと塩化水素が反応して白い煙(塩化アンモニウム)ができます。
集め方 アンモニアは、どのようにして集めますか?( 上方置換・下方置換・水上置換 )
上方置換 アンモニアは水に非常によく溶け、水上置換はできない。そこれ、空気よりも軽い性質を利用して上方置換で集める。
利用 アンモニアは大量に作られますが、主な利用目的は何?
肥料(化学肥料)
